2′-гидрокси-3′-нитро-3-бифенилкарбон қышқылы
2′-гидрокси-3′-нитро-3-бифенилкарбон қышқылы
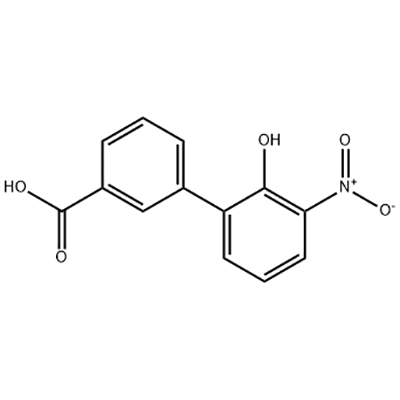
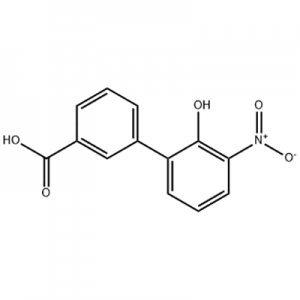
Элтромбопагтың аралық өнімі ретінде 2'-гидрокси-3'-нитро-3-бифенилкарбон қышқылы қолданылады.
Ұлыбританиядағы GlaxoSmithKline (GSK) әзірлеген және кейінірек Швейцариядағы Novartis компаниясымен бірлесіп әзірлеген Eltrombopag - әлемдегі алғашқы және жалғыз бекітілген шағын молекулалы пептидті емес TPO рецепторларының агонисті.Элтромбопаг 2008 жылы идиопатиялық тромбоцитопениялық пурпураны (ITP) емдеу үшін және 2014 жылы ауыр апластикалық анемияны (АА) емдеу үшін АҚШ FDA-мен мақұлданды.Бұл сонымен қатар соңғы 30 жылдағы АА емдеу үшін АҚШ FDA мақұлдаған алғашқы дәрі.
2012 жылдың желтоқсанында АҚШ FDA созылмалы С гепатиті (СГС) бар емделушілерде тромбоцитопенияны емдеуге арналған Элтромбопагты мақұлдады, осылайша тромбоциттер санының төмен болуына байланысты нашар болжамы бар С гепатиті бар емделушілер бауыр аурулары үшін интерферон негізіндегі стандартты терапияны бастай және сақтай алады.2014 жылдың 3 ақпанында GlaxoSmithKline FDA иммунотерапияға толық жауап бермеген ауыр химиялық кітаптағы апластикалық анемия (SAA) бар науқастарда гемопенияны емдеуге арналған Eltrombopag препаратының серпінді емдік дәрілік біліктілігін бергенін хабарлады.2015 жылдың 24 тамызында АҚШ FDA Eltrombopag препаратын кортикостероидтарға, иммуноглобулиндерге немесе спленэктомияға жеткіліксіз жауап беретін созылмалы иммундық тромбоцитопениясы (ITP) бар ересектер мен 1 жастан асқан балалардағы тромбоцитопенияны емдеу үшін мақұлдады.2018 жылдың 4 қаңтарында Элтромбопаг Қытайда бастапқы иммундық тромбоцитопенияны (ITP) емдеу үшін тізімге енгізілді.


![Касп унгин ацетаты;Каспофунгин ацетаты;Канцидтер;Каспофунгин ацетаты [USAN:BAN:JAN];](http://cdn.globalso.com/jindunchem-med/fbe17385-300x300.jpg)


![2-бутил-5-нитро-3-бензофуранил)[4-[3-(дибутилаМино)пропокси]фенил]](http://cdn.globalso.com/jindunchem-med/922e79ba.jpg)
